Physikalische Grundlagen im Kältekreislauf 1/3
Physikalische und thermodynamische Basics für Wärmepumpen und Kälteanlagen in drei Teilen (1/3)
In drei Teilen werden wir zusammen die verschiedenen Abläufe im Kältekreislauf einer Wärmepumpe oder Kälteanlagen betrachten. Aufbauend auf den Hauptsätzen der Thermodynamik betrachten wir die unterschiedlichen Aggregatszustandswechsel. Diese, sowie die kostenlose Umweltenergie, sind das Geheimnis, warum eine Wärmepumpe so effizient funktioniert, wenn die übrigen Randbedingungen erfüllt werden. Nachdem die Basics verstanden wurden, ist es Zeit tiefer in das log-p-h Diagramm für Kältemittel einzusteigen, alle Zustände, Temperaturen und Drücke sind von dort abzulesen (Teil 2). Im letzten Teil geht es um die Erhöhung der Betriebssicherheit und der Effizienz.
Für die sichere Planung, Installation und Inbetriebnahme ist es grundsätzlich ausreichend, die entsprechenden Normen, die technischen Regeln und die Installationsanleitungen der Hersteller zu beachten. Da wir aber Wärmepumpenspezialisten sind, müssen wir auch die physikalischen Zusammenhänge verstehen. Die thermodynamischen Grundlagen können dem ein oder anderen als etwas „trocken“ erscheinen, bilden aber die Basis, unter welchen Bedingungen eine Wärmepumpe richtig eingesetzt, betrieben und dann optimiert wird. Ich komme aus der „Kälte“ und mir fällt immer wieder auf, dass das Thema Kältetechnik bei dem Thema Wärmepumpen oft nur kurz angesprochen, nicht aber in der Tiefe behandelt wird.
Durch fehlendes Wissen können jedoch Fehler passieren, die es zu vermeiden gilt. Wärme ist eine Form der inneren Energie von Stoffen oder, thermodynamisch genauer, von Systemen. Hier bilden die vier Hauptsätze der Thermodynamik die Basis, welche elementar für das weitere Verständnis sind und hier unter Bezugnahme zur Kältetechnik/Wärmetechnik kurz erklärt werden. Zu beachten gilt, dass – physikalisch gesehen – keine Kälte existiert. In der Physik wird Wärme als ein molekularer Bewegungszustand der Materie definiert, der erst am absoluten Nullpunkt (T = 0 K, t = −273,15 °C) aufhört. Dementsprechend ist Kühlung nur durch Wärmeentzug möglich, nicht durch Zugabe von Kälte.
Wie war das gleich wieder mit den Hauptsätzen der Thermodynamik..?
Der nullte Hauptsatz wurde erst nach den anderen dreien entdeckt, da er aber fundamental für die Thermodynamik und die bestehenden Hauptsätze ist,
wurde er an den Anfang gestellt. Befindet sich System A mit System B und System B mit System C im thermischen Gleichgewicht, so befindet sich auch System C
mit System A im thermischen Gleichgewicht (Transitivität des Gleichgewichts). Dies erklärt, warum ein Thermometer, das in Kontakt mit dem zu messenden
Objekt steht, dessen Temperatur annimmt. Als weiteres Beispiel sei ein mit kochen dem Wasser gefülltes Gefäß genannt. Dies kühlt bei gewöhnlicher Umgebungstemperatur so lange ab, bis es die gleiche Temperatur wie die Umgebungsluft erreicht hat.
Der erste Hauptsatz der Thermodynamik ist auch bekannt als Energieerhaltungssatz. Die Kernaussage ist, dass in einem abgeschlossenen System die Summe aller Energien konstant ist. Energie kann weder erzeugt noch zerstört werden, es ist eine Gleichwertigkeit von Wärme und Arbeit gegeben. Arbeit lässt sich verlustfrei in Wärme umwandeln, umgekehrt ist dies ohne Verluste nicht möglich.
Der zweite Hauptsatz der Thermodynamik beschreibt die Richtung der Energieumwandlung, auch bekannt als der Entropiesatz der Thermodynamik. Wärme kann nie von selbst von einem Körper mit niedrigem Temperaturniveau auf einen Körper mit hohem Temperaturniveau übergehen. In der Kältetechnik bedeutet dies, dass die Verdampfungstemperatur niedriger sein muss als die Kaltwassertemperatur, um dem Kaltwasser die Wärme entziehen zu können. Als praktisches Beispiel gilt hier auch wieder der Topf mit kochendem Wasser. Stellt man diesen an die frische Luft, wird die Wärme vom wärmeren Wasser auf die kältere Luft übergehen, bis Wasser und Luft die gleiche Temperatur angenommen haben.
Der dritte Hauptsatz der Thermodynamik wird auch als Nernst’sches Wärmetheorem bezeichnet und macht die Aussage, dass es praktisch nicht möglich ist, die Temperatur eines Systems bis auf den absoluten Nullpunkt von 0 K, also −273,15 °C zu senken.
Aggregatszustandsänderungen – Erklärt am Beispiel von Wasser
Der kältetechnische/wärmetechnische Kreisprozess macht sich die Aggregatzustandsänderungen des Kältemittels zunutze. Dabei können relativ große Wärmemengen aufgenommen und wieder abgegeben werden, ohne die Temperatur zu ändern – es wird von latenter Wärme gesprochen. Vereinfacht gesagt: Diese Aggregatszustandsänderungen sind die zentralen Prozesse der Wärmeübertragung in einer Wärmepumpe. Da diese Aggregatzustände reversibel sind, ist ein Kreisprozess möglich.
Im Folgenden werden diese Aggregatzustandsänderungen zum leichteren Verständnis am Beispiel von Wasser bei Normdruck von 1,013 bar erklärt. Auf die Aggregatszustandsänderungen von fest in gasförmig (Sublimation) und gasförmig in fest (Resublimation) wird nicht näher eingegangen, da diese für Kompressionswärmepumpen nicht relevant sind. Sie werden nur der Vollständigkeit halber erwähnt.
Schmelzen und Erstarren
Führt man festen Körpern Wärme zu, können diese in den flüssigen Zustand übergehen. Die Wärmemenge, die ein Schmelzen des festen Körpers verursacht, wird
Schmelzwärme genannt. Um 1 kg Eis von 0 °C zu schmelzen, ist eine Wärmemenge von 333,4 kJ notwendig. Um dieses Wasser wieder in Eis zu verwandeln, ist erneut eine Wärmemenge von 333,4 kJ notwendig (Erstarrungswärme). Im Kreisprozess ist diese Aggregatzustandsänderung für uns nicht relevant. Das Erstarren kann aber indirekt erfolgen, sollte z. B. ein Verdampfer auf der Wasserseite auffrieren. Von Kindheit her ist uns aber das Schmelzen und Erstarren von Eis bzw. Wasser bekannt.
Verflüssigen (Kondensieren)
Wird dem trockenen, gesättigten Dampf die Verflüssigungswärme von 2.257 kJ entzogen, ist ein Aggregatzustandswechsel von gasförmig in flüssig zu beobachten.
Dies erfolgt wieder bei gleichbleibender Temperatur, also latent. Als praktisches Beispiel eignet sich ein Topf mit kochendem Wasser. Darüber wird eine kalte Metallplatte gehalten, die über Nacht bei z. B. 0 °C auf der Terrasse gelegen hat. Der heiße Dampf kondensiert an der kalten Platte, dem Dampf wird durch die kalte Platte Verflüssigungswärme entzogen, diese wird für den Phasenwechsel von gasförmig auf flüssig verwendet.
Verdampfen
Führt man einem Kilogramm Wasser von 0 °C ausreichend Wärme zu, steigt die Temperatur des Wassers beständig an, bis die Siedetemperatur (Siedepunkt) erreicht wird – man spricht von sensibler Wärme. Je Kelvin Temperaturerhöhung werden 4,19 kJ benötigt. Dementsprechend muss eine sensible Wärmemenge von 419 kJ zugeführt werden, um eine Temperatur von 100 °C zu erreichen. An diesem Siedepunkt beginnt das Wasser zu verdampfen. Nun muss die Verdampfungswärme 2.257 kJ zugeführt werden, um die Aggregatszustandsänderung von flüssig in gasförmig herbeizuführen. Die Enthalpie von 1 kg Wasserdampf bei 100 °C ergibt sich durch die Addition der sensiblen Wärmemenge von 419 kJ und der latenten Wärmemenge von 2.257 kJ und beträgt somit 2.676 kJ. Wird diesem trockenen gesättigten Dampf von 100 °C weiter Wärme zugeführt, so wird dieser überhitzt. Diese sensible Wärmezufuhr macht sich durch eine Temperaturerhöhung bemerkbar. Je Kelvin Temperaturerhöhung sind 1,86 kJ notwendig – dies entspricht der spezifischen Wärmekapazität des Wasserdampfs.
Dies war die „wissenschaftliche“ Abhandlung, in der Praxis möchten wir dies wie folgt erklären: Wird kochendem Wasser in einem Gefäß weiter Energie zugeführt, dann verdampft es, ohne dabei seine Temperatur zu erhöhen. Die Energiemenge, die in dieser Zustandsänderung (von flüssig auf gasförmig) steckt, ist das „Geheimnis“, mit der die Wärmepumpe aus einer „kalten“ Wärmequelle Energie auf nutzbarem Temperaturniveau gewinnt.

Kältekreislauf – Darstellung im log-p-h Diagramm
Der im vorhergehenden Kapitel beschriebene Phasenwechsel macht sich die Wärmepumpe im sogenannten Verdampfer- und Verflüssigerwärmeübertrager zunutze. Hinzu kommen unterschiedliche Druckniveaus, welche durch einen Verdichter und ein Expansionsventil erreicht werden. Als Medium in diesem reversiblen, abgeschlossenen Kreislauf wird Kältemittel verwendet. Um diesen Prozess besser verstehen zu können müssen wir tiefer in die Kältetechnik einsteigen. Leider bleiben uns hier die Theorie und entsprechende Diagramme nicht erspart. Wurde jedoch das Prinzip in der Tiefe verstanden, eröffnen sich hierdurch ungeahnte Möglichkeiten der Energieoptimierung.
Im Bild 1 sind die Hauptbauteile des Kältekreislaufes sowie die thermodynamischen Prozesse im log-p-h-Diagramm beispielhaft erklärt.
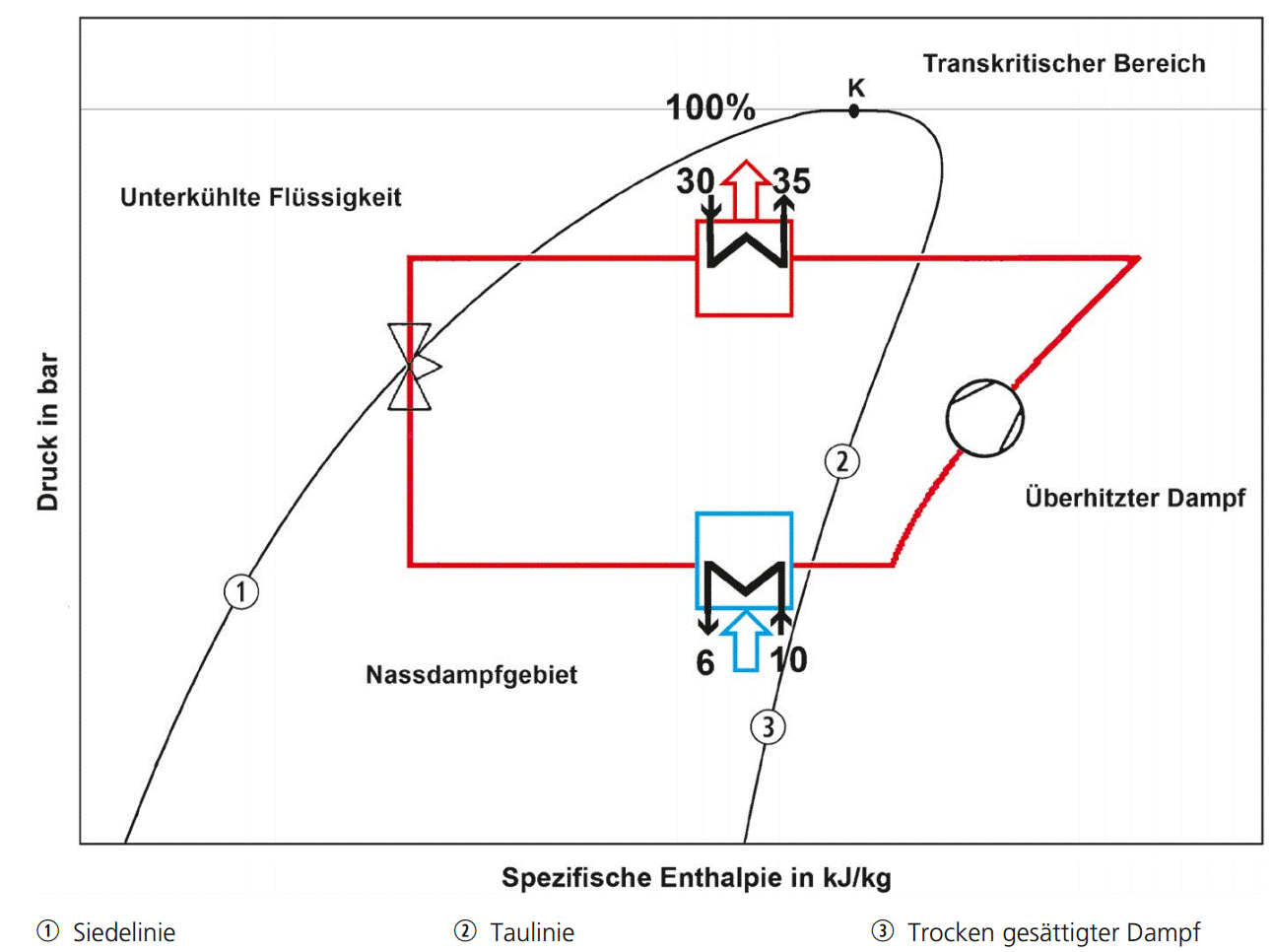
Bild 1: Hauptbestandteile einer Wärmepumpe dargestellt im log-p-h-Diagramm
In Bild 2 ist der Kältekreislauf mit dem Kältemittel R290 Propan bei −20 °C Verdampfungstemperatur und 77 °C Verflüssigungstemperatur dargestellt. Die entsprechenden Temperaturen und Drücke sind dem Diagramm zu entnehmen. Die im Diagramm ersichtlichen Isothermen, Isovaporen, Isochoren und Isentropen werden im nachfolgenden Kapitel näher erklärt.
Typ: Wer sich selber mit dem log-p-h Diagramm verschiedener Kältemittel beschäftigen möchte, findet bei TLK ENERGY ein sehr gutes und kostenfreies Programm.

Bild 2: Kältekreislauf R290 (Propan) im log-p-h-Diagramm (TLK Energy GmbH)
Das log-p-h-Diagramm
Um in der Kältetechnik Kompressionskälteprozesse darstellen und berechnen zu können, wird das log-p-h-Diagramm, auch Dampftafel genannt, angewendet. Jedes Diagramm ist nur für das jeweilige Kältemittel gültig und enthält dessen spezifische Stoffeigenschaften. Nachfolgend wird das Diagramm schrittweise erklärt, sodass am Ende des Kapitels die entsprechenden Betriebszustände aus dem Diagramm abgelesen werden können.
Auf der waagerechten Abszisse wird die spezifische Enthalpie h (in kJ/kg) abgelesen. Eine Linie mit gleichbleibender Enthalpie wird Isenthalpe genannt; in Bild 3 werden diese als blaue Geraden dargestellt. Vereinfacht gesagt macht die Enthalpie eine Aussage über die Wärmeenergie, die pro Kilogramm Kältemittel im jeweiligen Zustand (Druck und Temperatur) enthalten ist. Demnach kann ein Kältemittel mit unterschiedlicher Temperatur und unterschiedlichem Druck die gleiche Enthalpie besitzen, wenn sich dieser Zustand auf der gleichen Isenthalpen befindet. Entscheidend in der Wärmepumpentechnik ist die Enthalpie Differenz
der unterschiedlichen Zustände, nicht der absolute Wert. Die Differenz kann auf der x-Achse durch Subtraktion der Zustände ermittelt werden. Die Entspannung
des Kältemittels über das Expansionsventil wird bei gleichbleibender Enthalpie als senkrechte Gerade abgebildet.

Bild 3: Isenthalpen im log-p-h-Diagramm
Auf der senkrechten Ordinate (y-Achse) ist der Druck p (in bar) abzulesen. Da der Druck einen sehr großen Bereich (zwei bis drei Dekaden) abdeckt, erfolgt die
Darstellung zur kompakten Ansicht logarithmisch (log) und nicht linear. Folglich verlaufen Linien mit gleichbleibender Enthalpie senkrecht und Linien gleichbleibenden Drucks waagerecht. Da die Verdampfung und Kondensation bei gleichbleibendem Druck erfolgen, werden diese thermodynamischen Vorgänge mit waagerechten Linien dargestellt (Bild 4).
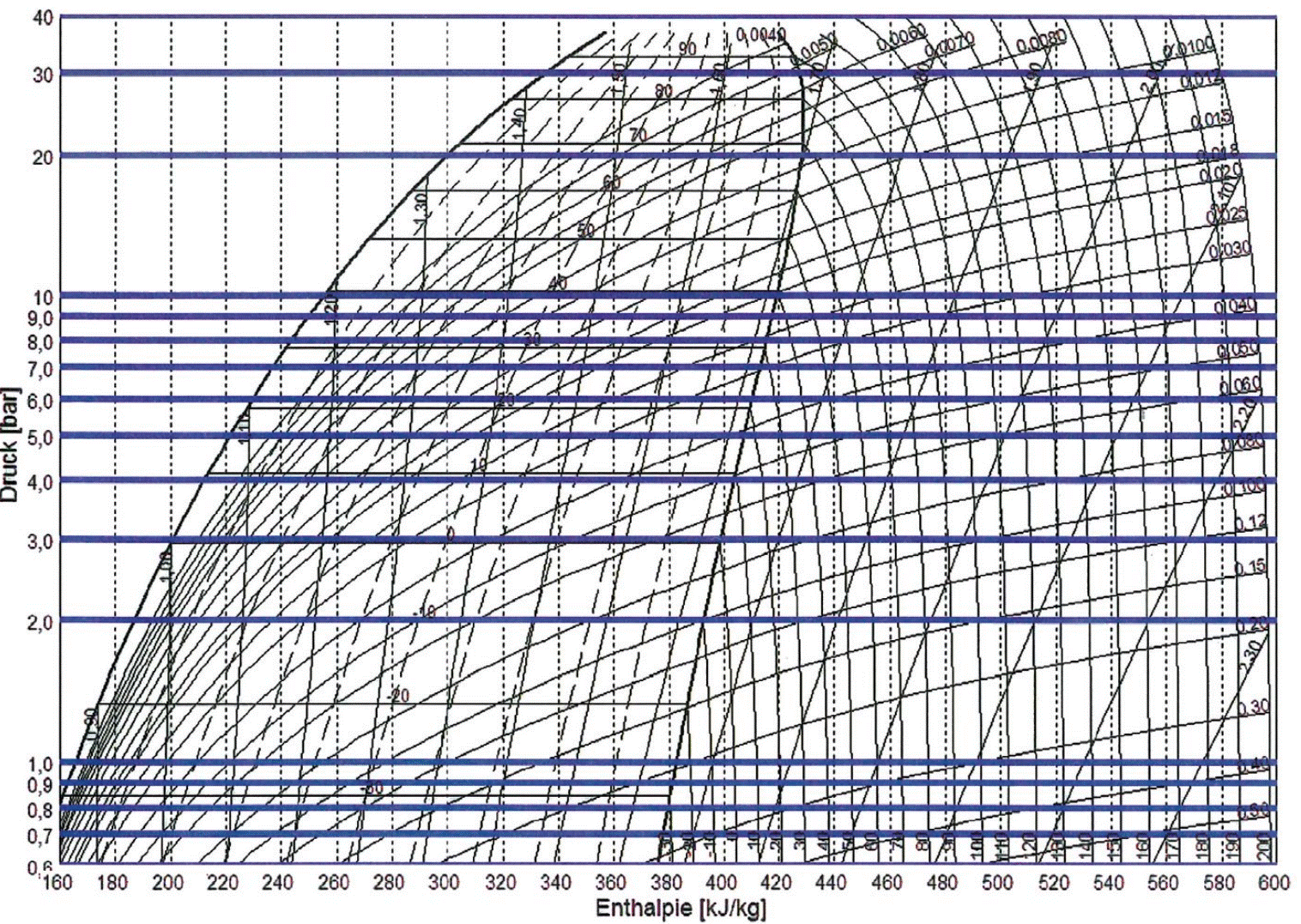
Bild 4: Isobare im log-p-h-Diagramm
Eine Linie mit konstanter Entropie s (in kJ/(kg · K)) wird Isentrope genannt (Bild 5) und ist eine stark ansteigende Gerade. Würde die Verdichtung adiabat erfolgen, also ohne Wärmeaustausch mit der Umgebung, wäre die Entropie konstant. Dies kann aber in der Praxis nicht erreicht werden. Es müssen Korrektur- und Gütegrade (Verluste) des Verdichters berücksichtigt werden. Es stellt sich eine Entropieerhöhung ein, dadurch krümmt sich die Gerade im oberen Bereich nach rechts weg (siehe Bild 1). Je geringer diese Krümmung, desto effizienter der Verdichter bzw. der Verdichtungsprozess.
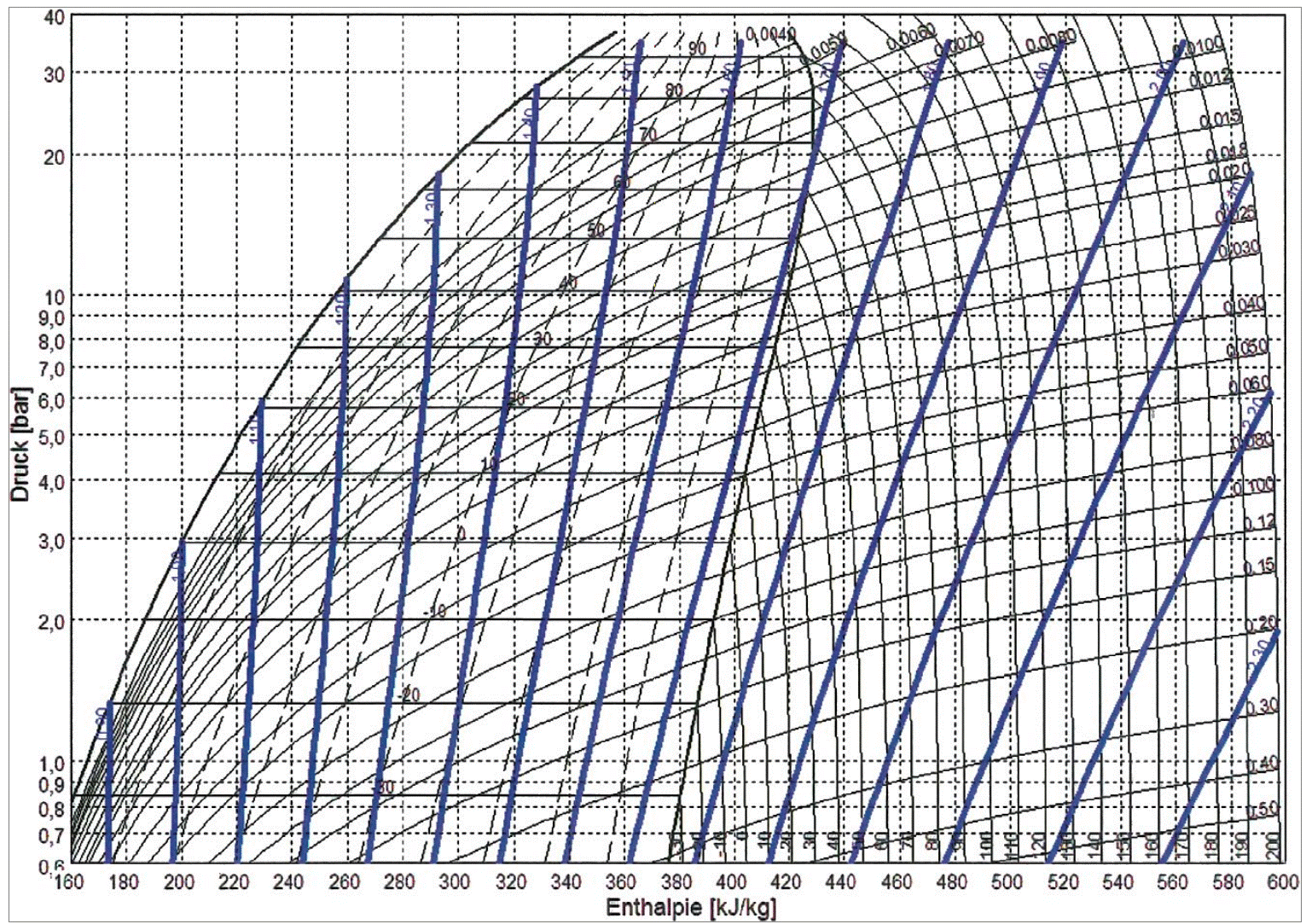
Bild 5: Isentrope im log-p-h-Diagramm
Eine Linie mit konstantem, spezifischen Volumen v (in m3/kg) wird Isochore genannt und ist eine nach rechts gekrümmte, leicht ansteigende Kurve. Bei der Expansion und Verdampfung steigt das spezifische Volumen, bei der Verdichtung und Verflüssigung nimmt es ab. Der Kehrwert des spezifischen Volumens ist die spezifische Dichte ρ (in kg/m3). Die Isochoren sind in Bild 6 dargestellt.
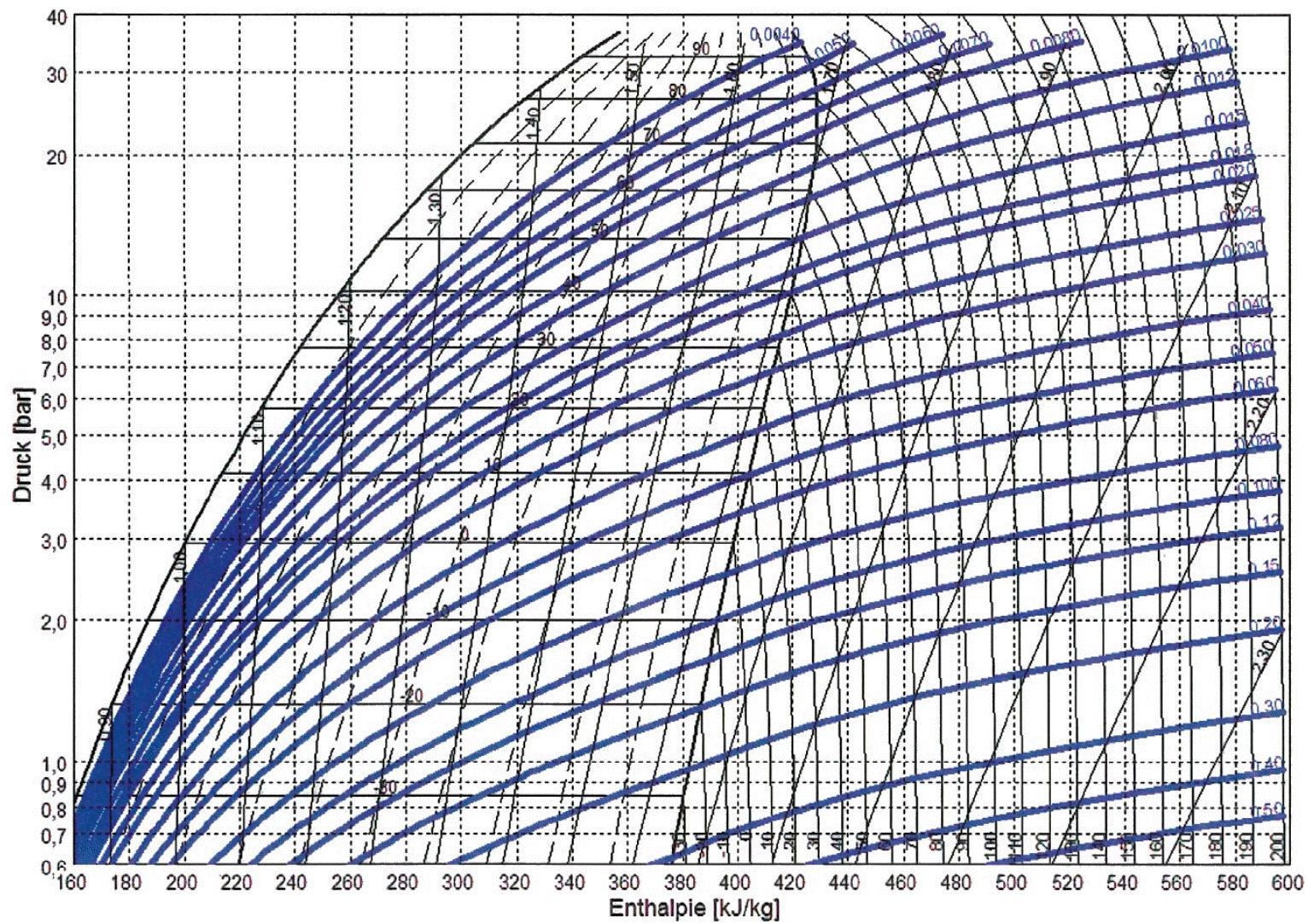
Bild 6: Isochore im log-p-h-Diagramm
Eine Linie mit konstanter Temperatur t (in °C) wird Isotherme (Bild 7) genannt. Diese fällt im Flüssigkeitsbereich nahezu senkrecht ab (also links von der
Grenzkurve), verläuft im zweiphasigen Nassdampfgebiet beim Phasenwechsel waagerecht (parallel zur Isobaren) und fällt im Gebiet des überhitzten Dampfes sehr
steil etwas nach rechts gekrümmt ab. Bei Kältemitteln, die ein Temperatur-Glide besitzen, verläuft die Gerade im zweiphasigen Gebiet leicht abfallend und nicht
waagerecht.

Bild 7: Isotherme im log-p-h-Diagramm
Die Dampftafeln geben also eine Auskunft über den Druck, die Temperatur, das spezifische Volumen und die Dichte, die spezifische Verdampfungsenthalpie sowie die Entropie eines Kältemittels. Reden wir von “Iso”, dann bedeutet dieses “Iso” soviel wie „gleichbleibend“ bzw. „konstant“. Die links vom kritischen Punkt liegende Kurve zeigt alle Zustandspunkte der siedenden Flüssigkeit auf, weswegen diese Kurve auch Siedelinie genannt wird. Die rechts vom kritischen Punkt liegende Kurve zeigt die Dampfzustände, diese Kurve wird auch Sattdampflinie genannt. Verbindet man diese beiden Kurven über den kritischen Punkt miteinander, erhält man die Grenzkurve eines Kältemittels.
An dieser Grenze haben die Gasphase und die flüssige Phase des Kältemittels die gleichen Eigenschaften (kritische Temperatur), Druck und Volumen fallen im kritischen Punkt zusammen. Oberhalb der kritischen Temperatur oder des kritischen Drucks existiert keine Trennung mehr zwischen Flüssig- und Gasphase (Bild 8).
K Kritischer Punkt 1 Siedelinie 2 Taulinie 3 Trocken, gesättigter Dampf 4 Gesättigte Flüssigkeit

Bild 8: Zustandsgebiete, Grenzkurve und kritischer Punkt im log-p-h-Diagramm
FAZIT
Was dem Klimatechniker sein h-x-Diagramm, ist dem Kältetechniker das log-p-h-Diagramm. Dieses ist kein Hexenwerk. Wer dies versteht, hat sich somit die Basis geschaffen, um Wärmepumpen und Kältemaschinen betreffend Funktionalität, Betriebssicherheit und Effizienz deutlich besser zu beurteilen. Wer noch tiefer in den Kältekreislauf und die Kältetechnik einsteigen möchte, dem empfehle ich das Buch Leitfaden für Kompressions- und Wasserkühlsätze
Im 2. Teil dieser Miniserie beschäftigen wir uns mit der Verdampfung, der Verdichtung, der Verflüssigung und der Expansion im Kältekreislauf. Die unterschiedlichen Zustände übertragen wir dann auf das log-p-h-Diagramm und vereinen dann die Theorie aus Teil 1 mit der Praxis im Teil 2.












